Chinese Journal of Tissue Engineering Research ›› 2013, Vol. 17 ›› Issue (18): 3397-3404.doi: 10.3969/j.issn.2095-4344.2013.18.023
Previous Articles Next Articles
Cell transplantation for the treatment of neurodegenerative diseases: “Transdifferentiation” appears?
Zhou Yu-feng, Zhang Fan-xi, Zhang Jian-min
- Department of Neurosurgery, 324th Hospital of PLA, Chongqing 400020, China
-
Received:2013-03-18Revised:2013-03-27Online:2013-04-30Published:2013-04-30 -
About author:Zhou Yu-feng★, Master, Associate chief physician, Department of Neurosurgery, 324th Hospital of PLA, Chongqing 400020, China zhouyufeng871@sina.com
CLC Number:
Cite this article
Zhou Yu-feng, Zhang Fan-xi, Zhang Jian-min. Cell transplantation for the treatment of neurodegenerative diseases: “Transdifferentiation” appears?[J]. Chinese Journal of Tissue Engineering Research, 2013, 17(18): 3397-3404.
share this article

2.1 细胞移植治疗神经变性疾病时的细胞类型 目前治疗神经变性疾病研究较多的细胞主要为自体干细胞移植及同种异体干细胞移植。用于神经系统疾病治疗的自体干细胞主要有骨髓干细胞、外周血干细胞及神经干细胞。自体干细胞的优势在于不存在移植排斥反应,但是因为来源于患者自身,疾病所致的内环境的改变有可能使干细胞的增殖分化能力受限。神经干细胞是一类存在于侧脑室下区等中轴部位并可自我更新的干细胞群。神经干细胞具有分化为神经元星形胶质细胞和少突胶质细胞的能力。在微环境的作用下,神经干细胞可定向分化为缺失的神经元,还可以建系长期保存,因此是细胞移植的理想材料。但目前神经干细胞面临分化效率低下的问题,且自体取材困难使其应用受限。异体干细胞主要有胚胎干细胞、异体骨髓干细胞及脐血干细胞。胚胎干细胞为全能干细胞,具有高度的分化能力,可以建系传代,增殖能力强,理论上有广泛的应用前景。但胚胎干细胞的使用存在着复杂的伦理道德及法律上的限制,同时目前尚不能控制胚胎干细胞在特定部位的分化,容易导致畸胎瘤的发生。异体骨髓干细胞和人脐血干细胞两者细胞成分相似,包含有造血干细胞、骨髓间充质干细胞及内皮祖细胞等。 近年来的研究显示,造血干细胞及骨髓间充质干细胞具有向神经细胞转分化的能力。有人发现体外培养的人骨髓来源的造血干细胞表达神经起源的转录因子及神经元和少突胶质细胞基因[2],人脐血来源的造血干细胞在体外可以“转分化”为神经元样细胞和神经胶质细胞[3]。骨髓间充质干细胞的体外及体内实验也显示其在某些诱导因子的作用下或体内内环境改变时具备向神经细胞转分化的能力[2, 4]。上述这些研究结果为造血干细胞和骨髓间充质干细胞在神经变性疾病中的应用提供了理论基础。近年来骨髓和脐血干细胞因其各自的优势而逐受重视,有望成为细胞移植治疗神经变性疾病的主要细胞来源。 骨髓干细胞的特点在于易采集、操作简单,如取自自体则不存在免疫排斥反应,较适合用于临床应用。但由于是成体干细胞,其增殖分化能力要低于胚胎及脐血干细胞。 脐血干细胞的成分与骨髓类似,但通过研究显示其内的造血干细胞增殖分化能力、体外集落形成能力及分泌生长因子的能力均强于骨髓;脐血造血干细胞的端粒及端粒酶的活性持续时间均长于骨髓;脐血T淋巴细胞较为原始且缺乏T淋巴细胞活化因子,抗原表达弱及不充分,NK细胞活性弱且存在CD4+和CD45RA+抑制性淋巴细胞,因此移植后引起免疫排斥反应较之骨髓概率要低,程度要轻;由于脐血免疫原性低,故也适合于HLA1-3个位点不合的无关供者的移植;脐血来源广泛,可长期保存;脐血受胎盘屏障的保护,细胞被病毒、细菌污染的概率低;脐血采集过程简单,对新生儿及产妇均无任何痛苦及不良作用,易被接受;脐血干细胞的应用不涉及社会、伦理及法律方面的争议[5]。 细胞移植治疗神经变性疾病常见的细胞还有异种细胞。目前认为猪胚胎神经组织是异种移植的最合适来源。猪脑结构上同灵长类动物脑类似,且有体积大、来源充足、易进行基因修饰等优点。猪脑移植目前面临感染和免疫排斥两个问题。移植使患者有感染病毒的可能,同时宿主能产生大量针对猪脑的抗体,免疫排斥也令人关注。虽有报道使用环孢素A、脱氧精胍菌素、他克莫司等可增加移植存活,但目前行异种细胞移植还存在不少困难[6]。 2.2 细胞移植治疗神经变性疾病时的基因修饰 细胞移植治疗神经变性疾病时的修饰基因主要有酪氨酸羟化酶、孤儿核受体、神经营养因子、Von Hippel-Lindau(VHL)基因、白细胞介素1及褪黑素。细胞移植治疗神经变性疾病时的基因修饰相关文献分析见表1。 酪氨酸羟化酶(Tyrosine hydroxylase,TH)是中脑黑质多巴胺合成的限速酶.是帕金森病基因治疗最早选择的目的基因。可通过神经干细胞、成纤维细胞、腺病毒、单纯疱疹病毒(HSV)等载体将阳基因移植到纹状体。通过增强脑内中脑黑质多巴胺的合成及外源性补充中脑黑质多巴胺神经元,对黑质及其周围微环境进行重建,改善动物模型的行为学异常。 孤儿核受体(nuclearrelated regulator-1,Nurr1)是目前尚未鉴定出配体的类同醇激素一甲状腺激素类寡核受体超家族的一员,也是一种转录因子类基因。Nurr1基因修饰后的胚胎干细胞分化为中脑黑质多巴胺神经元的比率可从15%增至50%[7]。"
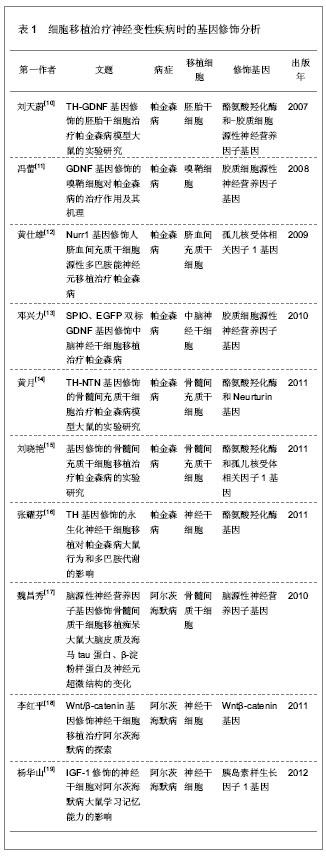

神经营养因子对中脑黑质多巴胺神经元具有保护作用,而且还对中脑黑质多巴胺神经元所处的微环境有一定的重建修复功能[8],这是其他移植治疗所没有的。其中 (GDNF)最受关注,胶质源性神经营养因子属于转化生长因子13(TGF-β)家族,是目前发现针对中脑黑质多巴胺神经元的一种最有效和特异性的神经营养因子[9]。同一家族的成员还包括Neurturin(NTN)、Persephin(PSP)、Artemin(ART)等。 Von Hippel-Lindau(VHL)基因具有调节转录、稳定细胞生长相关基因和调节细胞周期的功能。白细胞介素10及褪黑素均具有重要的免疫系统调节作用。目前,免疫调节蛋白或神经保护因子联合神经干细胞用于细胞移植后免疫应答的调节也是帕金森病细胞移植治疗研究的热点。 2.3 细胞移植治疗帕金森病 在2003至2012年10年间,CNKI数据库收录的细胞移植治疗帕金森病方面的研究文献共有463篇。发表相关文献较多的研究机构如下:复旦大学33篇,华中科技大学23篇,苏州大学21篇,第三军医大学20篇,山东大学16篇,首都医科大学14篇,昆明医学院13篇,郑州大学11篇,北京中日友好医院10篇,吉林大学10篇。这463篇文献中,有71篇由国家自然科学基金资助,18篇由国家重点基础研究发展计划(973计划)资助。 帕金森病是一种进行性神经系统退行性疾病,主要源于中脑黑质致密部多巴胺神经元退行性变导致的多巴胺与乙酰胆碱平衡失调。帕金森病主要的临床特征包括静止性震颤、肌强直、运动迟缓和姿势步态异常等,还可出现认知功能下降、情绪障碍等非运动症状。目前,帕金森病的发病机制尚未完全阐明,其治疗存在诸多困难。帕金森病的药物治疗早期一般采用以左旋多巴为主的替代治疗,病情加重后采用多巴胺受体激动剂直接兴奋多巴胺受体,细胞移植和基因治疗是正在探索而较有前景的新疗法。 细胞移植治疗帕金森病常见的细胞有骨髓干细胞、脐血干细胞、胚胎干细胞、神经干细胞、肾上腺髓质细胞、胎儿中脑腹侧组织细胞、异种细胞等。相关文献分析见表2。绝大多数细胞移植治疗帕金森病均采用移植到大鼠纹状体的方式。"


2.4 细胞移植治疗阿尔茨海默病 在2003至2012年10年间,CNKI数据库收录的细胞移植治疗阿尔茨海默病方面的研究文献共有135篇。发表相关文献较多的研究机构如下:郑州大学18篇,第三军医大学12篇,中国医科大学9篇,南方医科大学7篇,吉林大学5篇。这135篇文献中,有14篇由国家自然科学基金资助,3篇由国家高技术研究发展计划(863计划)资助。 阿尔茨海默病是一种进行性、退行性脑功能障碍综合征,阿尔茨海默病患者脑内Meynert核的胆碱能神经元发生明显的退行性病变。海马中的胆碱能神经元选择性丧失功能,大脑皮质中乙酰胆碱酯酶和胆碱乙酰化酶水平下降[27-28]。中枢神经系统原发性老化也是加剧脑神经发生退行性病变的原因。额叶皮质突触密度的降低,树突的萎缩和扩张,以小胶质细胞和星形胶质细胞为主的胶质增生反应都促进老化过程中大脑结构的改变[29]。目前,对阿尔茨海默病的治疗尚无很好的方法,主要用一些乙酰胆碱酯酶抑制剂类药物和神经保护因子来缓解症状。细胞移植治疗阿尔茨海默病还处于前期阶段。相关文献分析见表3。细胞移植治疗阿尔茨海默病的移植部位多为海马。 2.5 细胞移植治疗肌萎缩侧索硬化症 在2003至2012年10年间,CNKI数据库收录的细胞移植治疗肌萎缩侧索硬化方面的研究文献共有61篇。发表相关文献较多的研究机构如下:北京市虹天济神经科学研究院13篇,北京康复中心9篇,北京市西山医院8篇,泰山医学院6篇,中山大学5篇。这61篇文献中,有3篇由国家自然科学基金资助。 肌萎缩侧索硬化症又称为卢伽雷氏症,在1869年首次被描述。它是一种致死性运动神经元疾病,由于脊髓前角、脑干和额叶皮质运动神经元的进行性变性而引起相应的上运动神经元和下运动神经元损害表现。肌萎缩侧索硬化症的病因和发病机制尚未清楚,药物治疗和保护神经功能相结合仅能延长存活期,而无法恢复神经运动功能。近年来,病变区域的细胞移植被认为是一种最有前景的治疗措施。用于肌萎缩侧索硬化治疗的干细胞有胚胎干细胞、神经干细胞、骨髓间充质干细胞、脐带血非造血干细胞和诱导产生多能性干细胞等。相关文献分析见表4。细胞移植治疗肌萎缩侧索硬化的移植部位多为蛛网膜下腔。"

| [1] Hochgräfe K, Mandelkow EM. Making the Brain Glow: In Vivo Bioluminescence Imaging to Study Neurodegeneration. Mol Neurobiol. 2012.[2] Goolsby J, Marty MC, Heletz D, et al. Hematopoietic progenitors express neural genes. Proc Natl Acad Sci U S A. 2003;100(25):14926-14931.[3] Jang YK, Park JJ, Lee MC, et al. Retinoic acid-mediated induction of neurons and glial cells from human umbilical cord-derived hematopoietic stem cells. J Neurosci Res. 2004;75(4):573-584.[4] Ende N, Chen R, Ende-Harris D. Human umbilical cord blood cells ameliorate Alzheimer's disease in transgenic mice. J Med. 2001;32(3-4):241-247.[5] Larijani B, Esfahani EN, Amini P, et al. Stem cell therapy in treatment of different diseases. Acta Med Iran. 2012;50(2): 79-96.[6] Shamash S, Reichert F, Rotshenker S. The cytokine network of Wallerian degeneration: tumor necrosis factor-alpha, interleukin-1alpha, and interleukin-1beta. J Neurosci. 2002; 22(8):3052-3060.[7] Kim JH, Auerbach JM, Rodríguez-Gómez JA, et al. Dopamine neurons derived from embryonic stem cells function in an animal model of Parkinson's disease. Nature. 2002;418 (6893):50-56.[8] Chen X, Liu W, Guoyuan Y, et al. Protective effects of intracerebral adenoviral-mediated GDNF gene transfer in a rat model of Parkinson's disease. Parkinsonism Relat Disord. 2003;10(1):1-7.[9] McGrath J, Lintz E, Hoffer BJ, et al. Adeno-associated viral delivery of GDNF promotes recovery of dopaminergic phenotype following a unilateral 6-hydroxydopamine lesion. Cell Transplant. 2002;11(3):215-227.[10] 刘天蔚.TH-GDNF基因修饰的胚胎干细胞治疗帕金森病模型大鼠的实验研究[D].山东:青岛大学,2007.[11] 冯蕾.GDNF基因修饰的嗅鞘细胞对帕金森病的治疗作用及其机理[D].山东:山东大学,2008.[12] 黄仕雄.Nurr1基因修饰人脐血间充质干细胞源性多巴胺能神经元移植治疗帕金森病[J]中山大学学报(医学科学版),2009, 30(05):522-526.[13] 邓兴力,王应莉,杨智勇,等.SPIO、EGFP双标GDNF基因修饰中脑神经干细胞移植治疗帕金森病[J].中风与神经疾病杂志,2010, 27(02):109-113.[14] 黄月.TH-NTN基因修饰的骨髓间充质干细胞治疗帕金森病模型大鼠的实验研究[D].河南:郑州大学,2011.[15] 刘晓艳,康慧聪,胡琦,等.基因修饰的骨髓间充质干细胞移植治疗帕金森病的实验研究[J]. 华中科技大学学报(医学版),2011, 40(04):396-399.[16] 张耀芬,李振洲,郑静晨,等.TH基因修饰的永生化神经干细胞移植对帕金森病大鼠行为和多巴胺代谢的影响[J].武警医学,2011, 22(01):34-37,42.[17] 魏昌秀,代宏,陈松林.脑源性神经营养因子基因修饰骨髓间质干细胞移植痴呆大鼠大脑皮质及海马tau蛋白、β-淀粉样蛋白及神经元超微结构的变化[J].中国组织工程研究与临床康复, 2010, 14(45):8421-8425.[18] 李红平,康朝胜,余资江,等.Wnt/β-catenin基因修饰神经干细胞移植治疗阿尔茨海默病的探索[J].四川解剖学杂志,2011,19(04): 42-45.[19] 杨华山,王金国,蒋莉.IGF-1修饰的神经干细胞对阿尔茨海默病大鼠学习记忆能力的影响[J].中国老年学杂志,2012,32(20): 4465-4467.[20] 高华,王玉玲,杨新玲.脂肪来源的神经干细胞移植治疗帕金森病模型鼠[J].中华实验外科杂志,2012,29(03):462-465.[21] 张艳华,卢蕾,董静,等.X盒结合蛋白1转染神经干细胞移植帕金森大鼠黑质中相关递质及核蛋白的表达[J].中国组织工程研究, 2012,16(45):8510-8513.[22] 樊志刚,刘芳.脐血干细胞移植对帕金森病大鼠旋转行为的影响[J].中国组织工程研究,2012,16(14):2567-2570.[23] 王家增.携带绿色荧光蛋白基因的神经上皮干细胞移植治疗帕金森病[J].中国组织工程研究,2012,16(06):1080-1084.[24] 周辉,盛汉松,许尚虞,等.多能成体祖细胞移植治疗帕金森病及其作用机制[J].中华实验外科杂志,2011,28(11):1935-1938.[25] 邱云,汪铮,路红社,等.脐带间充质干细胞移植治疗帕金森病8例[J].中国组织工程研究与临床康复,2011,15(36): 6833-6836.[26] 周井铎,邬巍,郭云宝,等.GDNF修饰脂肪间质干细胞移植治疗帕金森病模型大鼠的实验研究[J].中国老年学杂志,2011, 31(12): 2269-2271.[27] Auld DS, Kornecook TJ, Bastianetto S, et al. Alzheimer's disease and the basal forebrain cholinergic system: relations to beta-amyloid peptides, cognition, and treatment strategies. Prog Neurobiol. 2002;68(3):209-245.[28] German DC, Yazdani U, Speciale SG, et al. Cholinergic neuropathology in a mouse model of Alzheimer's disease. J Comp Neurol. 2003;462(4):371-381.[29] Limke TL, Rao MS. Neural stem cells in aging and disease. Cell Mol Med. 2002;6(4):475-496.[30] 牟心红,张岭,张玥,等.骨髓间充质干细胞移植对老年性痴呆大鼠学习和记忆能力的影响[J].武警后勤学院学报(医学版),2012, 21 (07):499-502,封2.[31] 王清华,徐如祥,长尾省吾.胚胎干细胞在阿尔茨海默病小鼠中的移植研究[J].中华神经医学杂志,2011,10(05):464-466.[32] 王丽娟.脐血间充质干细胞移植对阿尔茨海默病大鼠行为学的影响[J].中国老年学杂志,2012,32(21):4687-4689.[33] 马刘红,程欣,徐建乒,等.人脐带间充质干细胞对阿尔茨海默病模型小鼠学习记忆能力的影响[J].广东医学,2012,33(10): 1366-1369.[34] 陈双庆,蔡庆,沈玉英,等.神经干细胞移植治疗APP-PS1转基因阿尔茨海默病小鼠的1H-MR波谱研究[J].中华放射学杂志,2012, 46(02):164-169.[35] 王萌,李瑞花,吴菊平,等.神经干细胞与嗅成鞘细胞共培养共移植对大鼠阿尔茨海默病的影响[J].山西医药杂志(下半月版),2012, 41(01):23-26[36] 赖福生,卢少军,王一芳,等.脐带血有核细胞移植治疗肌萎缩侧索硬化的临床研究[J].东南国防医药,2010,12(06):515-518.[37] 杨志刚,杨春水,李建英,等.脐血源间充质干细胞治疗肌萎缩侧索硬化的临床研究[J].中外医疗,2012,31(21):68-69.[38] 梁豪文,杨佳勇,杨万章,等.脐血源神经干细胞移植治疗肌萎缩侧索硬化症[J].中西医结合心脑血管病杂志,2007,5(06):493-495.[39] 赵翠萍,张成,黄慧,等.人骨髓间质干细胞治疗肌萎缩侧索硬化症模型小鼠的行为学和病理学研究[J].中国病理生理杂志,2010, 26(01):101-106.[40] 黄红云,王洪美,顾征,等.嗅鞘细胞移植治疗运动神经元病/肌萎缩侧索硬化的初步报告[J]. 中国临床康复,2004,8(13): 2440-2441.[41] 孙大勇,韩杰,李雪娇,等.自体外周血干细胞移植治疗肌萎缩侧索硬化患者9例:短期效果分析[J].中国组织工程研究,2012,16(14): 2645-2647[42] 金善,邵福源.干细胞移植治疗神经变性疾病[J].中华神经医学杂志,2007,6(01):89-92.[43] Stone JG, Siedlak SL, Tabaton M, et al. The cell cycle regulator phosphorylated retinoblastoma protein is associated with tau pathology in several tauopathies. J Neuropathol Exp Neurol. 2011;70(7):578-587.[44] Lenzken SC, Romeo V, Zolezzi F, et al. Mutant SOD1 and mitochondrial damage alter expression and splicing of genes controlling neuritogenesis in models of neurodegeneration. Hum Mutat. 2011;32(2):168-182.[45] Dunkel P, Chai CL, Sperlágh B, et al. Clinical utility of neuroprotective agents in neurodegenerative diseases: current status of drug development for Alzheimer's, Parkinson's and Huntington's diseases, and amyotrophic lateral sclerosis. Expert Opin Investig Drugs. 2012;21(9): 1267-1308. [46] Kanouchi T, Ohkubo T, Yokota T. Can regional spreading of amyotrophic lateral sclerosis motor symptoms be explained by prion-like propagation? J Neurol Neurosurg Psychiatry. 2012;83(7):739-745.[47] Yamamoto-Watanabe Y, Watanabe M, Jackson M, et al. Quantification of cystatin C in cerebrospinal fluid from various neurological disorders and correlation with G73A polymorphism in CST3. Brain Res. 2010;1361:140-145.[48] Ambegaokar SS, Roy B, Jackson GR. Neurodegenerative models in Drosophila: polyglutamine disorders, Parkinson disease, and amyotrophic lateral sclerosis. Neurobiol Dis. 2010;40(1):29-39. |
| [1] | Wang Haiying, Lü Bing, Li Hui, Wang Shunyi. Posterior lumbar interbody fusion for degenerative lumbar spondylolisthesis: prediction of functional prognosis of patients based on spinopelvic parameters [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(9): 1393-1397. |
| [2] | Ji Zhixiang, Lan Changgong. Polymorphism of urate transporter in gout and its correlation with gout treatment [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1290-1298. |
| [3] | Li Jiacheng, Liang Xuezhen, Liu Jinbao, Xu Bo, Li Gang. Differential mRNA expression profile and competitive endogenous RNA regulatory network in osteoarthritis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1212-1217. |
| [4] | Tan Jingyu, Liu Haiwen. Genome-wide identification, classification and phylogenetic analysis of Fasciclin gene family for osteoblast specific factor 2 [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(8): 1243-1248. |
| [5] | Wang Xianyao, Guan Yalin, Liu Zhongshan. Strategies for improving the therapeutic efficacy of mesenchymal stem cells in the treatment of nonhealing wounds [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1081-1087. |
| [6] | Wan Ran, Shi Xu, Liu Jingsong, Wang Yansong. Research progress in the treatment of spinal cord injury with mesenchymal stem cell secretome [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1088-1095. |
| [7] | Xie Wenjia, Xia Tianjiao, Zhou Qingyun, Liu Yujia, Gu Xiaoping. Role of microglia-mediated neuronal injury in neurodegenerative diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1109-1115. |
| [8] | Li Shanshan, Guo Xiaoxiao, You Ran, Yang Xiufen, Zhao Lu, Chen Xi, Wang Yanling. Photoreceptor cell replacement therapy for retinal degeneration diseases [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1116-1121. |
| [9] | Zeng Yanhua, Hao Yanlei. In vitro culture and purification of Schwann cells: a systematic review [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1135-1141. |
| [10] | Geng Yao, Yin Zhiliang, Li Xingping, Xiao Dongqin, Hou Weiguang. Role of hsa-miRNA-223-3p in regulating osteogenic differentiation of human bone marrow mesenchymal stem cells [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1008-1013. |
| [11] | Zou Gang, Xu Zhi, Liu Ziming, Li Yuwan, Yang Jibin, Jin Ying, Zhang Jun, Ge Zhen, Liu Yi. Human acellular amniotic membrane scaffold promotes ligament differentiation of human amniotic mesenchymal stem cells modified by Scleraxis in vitro [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1037-1044. |
| [12] | Guan Qian, Luan Zuo, Ye Dou, Yang Yinxiang, Wang Zhaoyan, Wang Qian, Yao Ruiqin. Morphological changes in human oligodendrocyte progenitor cells during passage [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1045-1049. |
| [13] | Wang Hanyue, Li Furong, Yang Xiaofei, Hu Chaofeng. Direct reprogramming hepatocytes into islet-like cells by efficiently targeting and activating the endogenous genes [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1056-1063. |
| [14] | Wang Feng, Zhou Liyu, Saijilafu, Qi Shibin, Ma Yanxia, Wei Shanwen. CaMKII-Smad1 promotes axonal regeneration of peripheral nerves [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1064-1068. |
| [15] | Liu Cong, Liu Su. Molecular mechanism of miR-17-5p regulation of hypoxia inducible factor-1α mediated adipocyte differentiation and angiogenesis [J]. Chinese Journal of Tissue Engineering Research, 2021, 25(7): 1069-1074. |
| Viewed | ||||||
|
Full text |
|
|||||
|
Abstract |
|
|||||

